1. 기초 지식 (실험 부분을 보고 싶으시면 바로 2부로 옮겨주세요)
Real time PCR은 기존 PCR의 파생 반응으로 주로 형광 신호의 변화를 통해 PCR 증폭 반응의 각 사이클에서 증폭 산물의 양 변화를 실시간으로 모니터링하고 ct 값과 표준 곡선의 관계를 통해 시작 템플릿을 정량적으로 분석합니다.
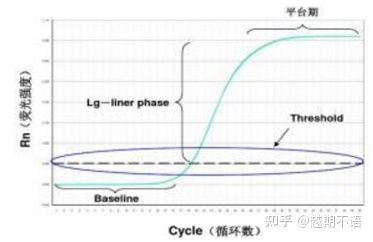
RT-PCR의 특정 데이터는 다음과 같습니다.기준선, 형광 역치그리고CT 값.
| 기준선: | 3~15주기의 형광값이 기준선(baseline)으로, 간헐적인 측정 오차로 인해 발생한다. |
| 임계값(임계값): | 증폭 곡선의 지수 성장 영역에서 적절한 위치에 설정된 형광 검출 한계를 말하며 일반적으로 기준선의 표준 편차의 10배입니다. |
| CT 값: | 각 반응 튜브의 형광 값이 임계값에 도달했을 때의 PCR 사이클 수입니다. Ct 값은 초기 템플릿의 양에 반비례합니다. |
RT-PCR의 일반적인 라벨링 방법:
| 방법 | 이점 | 결점 | 적용 범위 |
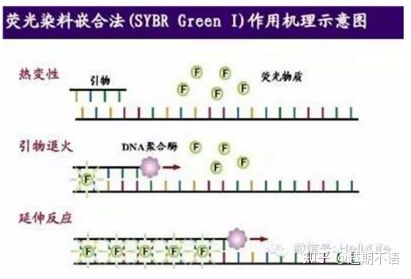
| SYBR 그린Ⅰ | 넓은 적용성, 민감하고 저렴하며 편리함 | 프라이머 요구 사항이 높고 비특정 밴드가 발생하기 쉽습니다. | 다양한 표적 유전자의 정량 분석, 유전자 발현 연구, 형질전환 재조합 동식물 연구에 적합합니다. |
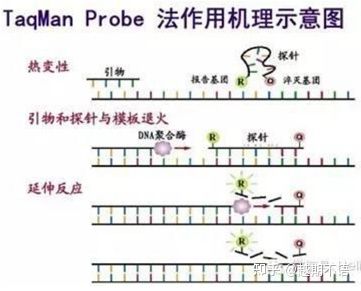
| 태크맨 | 우수한 특이성 및 높은 반복성 | 가격이 비싸고 특정 목표에만 적합합니다. | 병원체 검출, 약제내성 유전자 연구, 약제효능평가, 유전질환 진단 |
| 분자 표지 | 높은 특이성, 형광성, 낮은 background | 가격이 비싸고 특정 용도에만 적합하며 디자인이 어렵고 가격이 높습니다. | 특정 유전자 분석, SNP 분석 |
2. 실험 단계
2.1 실험 그룹화 정보- 그룹에 웰이 여러 개 있어야 하며 생물학적 반복이 있어야 합니다.
| ① | 블랭크 컨트롤 | 실험에서 세포 성장 상태를 감지하는 데 사용 |
| ② | 음성 대조군 siRNA(비특이적 siRNA 서열) | RNAi 작용의 특이성을 입증합니다.siRNA는 200nM 농도에서 비특이적 스트레스 반응을 유도할 수 있습니다. |
| ③ | 형질감염 시약 제어 | 세포에 대한 형질주입 시약의 독성 또는 표적 유전자의 발현에 대한 영향 배제 |
| ④ | 표적 유전자에 대한 siRNA | 표적 유전자 발현 억제 |
| ⑤ (선택사항) | 양성 siRNA | 실험 시스템 및 운영 문제를 해결하는 데 사용 |
| ⑥ (선택사항) | 형광 제어 siRNA | Cell transfection의 효율성은 현미경으로 관찰할 수 있습니다. |
2.2 프라이머 디자인의 원리
| 증폭 조각 크기 | 바람직하게는 100-150bp |
| 프라이머 길이 | 18-25bp |
| GC 내용 | 30%-70%, 바람직하게는 45%-55% |
| Tm 값 | 58-60℃ |
| 순서 | 지속적인 T/C를 피하십시오.A/G 연속 |
| 3 종료 시퀀스 | GC 풍부 또는 AT 풍부를 피하십시오.말단 염기는 바람직하게는 G 또는 C이고;T를 피하는 것이 가장 좋습니다. |
| 상보성 | 프라이머 내 또는 두 프라이머 사이에 3개 이상의 염기로 상보적인 서열을 피하십시오. |
| 특성 | 폭발 검색을 사용하여 프라이머 특이성 확인 |
①SiRNA는 종 특이적이며 다른 종의 서열은 다를 것입니다.
②SiRNA는 동결건조 분말 형태로 포장되어 있어 상온에서 2~4주간 안정적으로 보관할 수 있습니다.
2.3 미리 준비해야 하는 도구 또는 시약
| 프라이머(내부 참조) | 정방향 및 역방향 2개 포함 |
| 프라이머(표적 유전자) | 정방향 및 역방향 2개 포함 |
| 표적 Si RNA(3개 스트립) | 일반적으로 회사는 3개의 스트립을 합성한 후 RT-PCR로 3개 중 하나를 선택합니다. |
| 트랜스펙션 키트 | Lipo2000 등 |
| RNA 신속 추출 키트 | transfection 후 RNA 추출용 |
| 신속한 역전사 키트 | cDNA 합성을 위한 |
| PCR 증폭 키트 | 2×슈퍼 SYBR 그린 qPCR 마스터 믹스 |
2.4 특정 실험 단계에서 주의를 기울여야 하는 문제:
①siRNA transfection 과정
1. 플레이팅의 경우 24-well plate, 12-well plate 또는 6-well plate를 선택할 수 있으며(24-well plate의 각 well에 제안된 평균 RNA 농도는 약 100-300 ng/uL임) 세포의 최적 transfection 밀도는 최대 60%-80% 정도입니다.
2. 형질 감염 단계 및 특정 요구 사항은 지침을 엄격히 준수합니다.
3. transfection 후, mRNA 검출(RT-PCR)을 위해 24-72시간 이내에 샘플을 수집하거나 48-96시간 이내에 단백질 검출(WB)을 할 수 있습니다.
② RNA 추출 과정
1. 외인성 효소에 의한 오염을 방지한다.주로 마스크와 장갑을 엄격하게 착용하는 것을 포함합니다.멸균 피펫 팁 및 EP 튜브 사용;실험에 사용된 물은 RNase-Free여야 합니다.
2. 빠른 추출 키트에 제시된 두 번 수행하는 것이 좋습니다. 이렇게 하면 순도와 수율이 크게 향상됩니다.
3. 폐액이 RNA 컬럼에 닿지 않아야 합니다.
③ RNA 정량
RNA를 추출한 후 Nanodrop으로 직접 정량할 수 있으며 최소 판독값은 10ng/ul까지 낮을 수 있습니다.
④역전사 과정
1. RT-qPCR의 높은 민감도로 인해 후속 Ct가 너무 다르거나 SD가 통계 분석을 위해 너무 커지는 것을 방지하기 위해 각 샘플에 대해 최소 3개의 병렬 웰을 만들어야 합니다.
2. 마스터 믹스를 반복적으로 동결 및 해동하지 마십시오.
3. 각 튜브/구멍을 새 팁으로 교체해야 합니다!샘플을 추가하기 위해 동일한 피펫 팁을 계속 사용하지 마십시오!
4. 샘플을 첨가한 후 96웰 플레이트에 부착된 필름을 플레이트로 평활화해야 합니다.튜브 벽의 액체가 아래로 흘러 기포를 제거할 수 있도록 기계에 넣기 전에 원심 분리하는 것이 가장 좋습니다.
⑤공통 곡선 분석
| 로그 성장 기간 없음 | 템플릿 농도가 높을 수 있음 |
| CT 값 없음 | 형광 신호 감지를 위한 잘못된 단계; 프라이머 또는 프로브의 분해 - 무결성은 PAGE 전기영동으로 감지할 수 있습니다. 템플릿 양이 부족합니다. 템플릿의 열화 - 샘플 준비에서 불순물의 도입과 반복적인 동결 및 해동을 방지합니다. |
| Ct>38 | 낮은 증폭 효율;PCR 제품이 너무 깁니다.다양한 반응 성분이 분해됩니다. |
| 선형 증폭 곡선 | 프로브는 반복된 동결-해동 주기 또는 장기간 빛에 노출되면 부분적으로 저하될 수 있습니다. |
| 중복 구멍의 차이가 특히 큽니다. | 반응용액이 완전히 녹지 않거나 혼합되지 않는 경우;PCR 기기의 열탕이 형광 물질로 오염된 경우 |
2.5 데이터 분석 정보
qPCR의 데이터 분석은 상대 정량화와 절대 정량화로 나눌 수 있습니다.예를 들어, 대조군의 세포와 비교한 치료군의 세포,
X 유전자의 mRNA가 몇 번이나 변하는지, 이것은 상대적 정량화입니다.특정 수의 세포에서 X 유전자의 mRNA
얼마나 많은 사본이 있는지, 이것은 절대 정량화입니다.일반적으로 우리가 실험실에서 가장 많이 사용하는 방법은 상대정량법입니다.대개,2-ΔΔct 방법실험에서 가장 많이 사용되는 방법이므로 여기서는 이 방법에 대해서만 자세히 소개한다.
2-ΔΔct 방법: 얻어진 결과는 대조군의 표적 유전자에 대한 실험군의 표적 유전자 발현의 차이이다.표적 유전자와 내부 참조 유전자의 증폭 효율이 모두 100%에 가까워야 하고 상대편차가 5%를 넘지 않아야 한다.
계산 방법은 다음과 같습니다.
Δct 대조군 = 대조군 내 표적 유전자의 ct 값 – 대조군 내 내부 참조 유전자의 ct 값
Δct 실험군 = 실험군 대상 유전자의 ct 값 – 실험군 내부 참조 유전자의 ct 값
ΔΔct=Δct 실험군-Δct 대조군
마지막으로 표현 수준 차이의 배수를 계산합니다.
Change Fold=2-ΔΔct (엑셀 함수에 해당하는 것은 POWER임)
관련 상품:
게시 시간: 2023년 5월 20일